
コンテンツ
単純に計算するために、化学者は、反応やその他の化学プロセスに関与する特定の化合物の原子数の標準単位を作成しました。彼らは、1モル(mol)を、12グラムの炭素12と同じ数の基本単位を持つ物質の量として定義します。これは、アボガドロス数(6.022×10)です。23)。 SI(メートル法)測定システムでは、ミリモル(Mmol)を1000分の1モルと定義しています。通常、手持ちの量を量って物質のモル数を計算します。 Mmolに変換する場合は、10を掛けます3 (1,000).
TL; DR(長すぎる;読まなかった)
1モルは、特定の化合物の粒子のアボガドロス数に等しい。 1ミリモル(Mmol)は1000分の1モルです。
ほくろの計算方法
原子質量は、原子質量単位(AMU)で測定されます。 1つのAMUは、基底状態の炭素12原子の核の質量のちょうど1/12です。物質の1モルは、その物質の粒子のアボガドロス数に等しいと定義されています。この定義によると、グラム単位の物質の1モルの重量は、AMU内のその物質の個々の粒子の重量と同じ数です。たとえば、炭素12の原子量は12 AMUであるため、炭素12の1モルの重量は12グラムです。
水素ガス(H2)。コンテナ内の各粒子は2つの水素原子で構成される分子であるため、分子量を計算するために必要なのは水素の原子質量のみです。周期表のほとんどのバージョンは、そのシンボルの下に各元素の原子質量をリストしています。原子核に単一のプロトンを持つ水素の場合、1.008 AMUは、水素のすべての天然に存在する同位体の平均です。その結果、水素ガスの原子質量は2.016 AMUであり、1モルの水素ガスの重量は2.016グラムです。サンプルのモル数を調べるには、サンプルをグラム単位で計量し、その重量を水素ガスの分子量(グラム単位)で除算します。たとえば、15グラムの純粋な水素ガスのサンプルには7.44モルが含まれています。
Mmolへの変換
調査中の数量が非常に少ないため、モルで表現するのは面倒です。ミリモルを入力します。ほくろの数に1000を掛けることで、非常に小さな数をより扱いやすい数に変換できます。これは、ミリリットルのオーダーでボリューム単位を扱う場合に特に便利です。
1 mol = 1,000 Mmol
溶液濃度
化学者は、溶液中の特定の化合物の濃度の尺度としてモル濃度を使用します。モル濃度は、リットルあたりのモル数として定義されます。 1,000を掛けて、モル濃度をミリモル濃度に変換します。たとえば、1モル(モル、Mと表記)溶液の濃度は1リットルあたり1モルです。これは、1,000 Mmol(ミリモル、mMと表記されることもある)溶液に相当します。これは、1リットルあたり1,000 Mmolを含む溶液です。
例
溶液には0.15グラムの炭酸カルシウムが含まれています。それは何ミリモルですか?
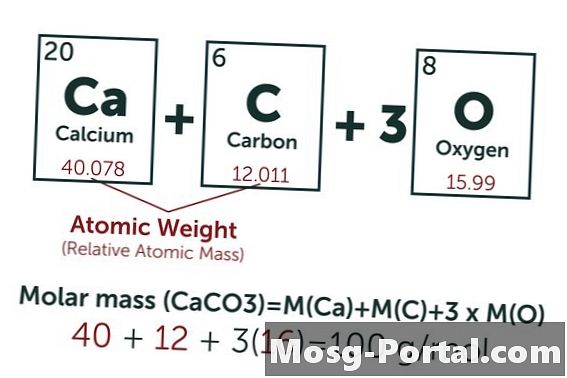
炭酸カルシウムの化学式はCaCOです3。炭素(C)の原子量は約12 AMU、酸素(O)の原子量は約16 AMU、カルシウム(Ca)の原子量は約40 AMUです。したがって、炭酸カルシウムの各分子の重量は100 AMUです。つまり、1モルの重量は約100グラムです。 0.15グラムの重量は、0.15 g÷100 g / mol = 0.0015モルを表します。これは1.5 Mmolに相当します。
2.5リットルの溶液中のこのくらいの炭酸カルシウムのモル濃度とミリモル濃度は何ですか?
モル濃度は1リットルあたりのモル数として定義されているため、モル数を2.5で割るとモル濃度が得られます。0.0015÷2.5 =
0.0006 M
1,000で乗算して、ミリモル濃度を取得します=
0.6 mM
ミリモル数を溶液の体積で割ると、ミリモル濃度で同じ結果が得られることに注意してください。