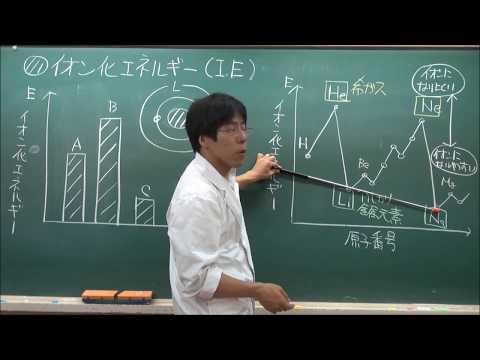
 ビデオ: 【化学基礎】イオン化エネルギー
ビデオ: 【化学基礎】イオン化エネルギー
コンテンツ
強酸と強塩基は水中で完全にイオン化します。つまり、各酸性分子からの水素イオンまたは各アルカリ分子からの水酸化物イオンが分離または供与されます。ただし、フッ化水素酸などの弱酸やアンモニアなどの弱塩基は、限られた量の水中でイオン化します。水中の解離またはイオン化された酸または塩基の割合を計算するのはかなり簡単で、特定の弱酸と弱塩基の挙動を理解するのに役立ちます。
溶液中の解離(イオン化)酸または塩基の量を決定します。多くの場合、この情報は問題に含まれています。より高度なクラスにいる場合は、実験研究またはフォーミュラチェーンを使用して、水素または水酸化物イオンの量を計算する必要があります。
酸または塩基の初期濃度(1リットルあたりのモル数)で示される、解離した酸または塩基の量(1リットルあたりのモル数の単位で表示)を割ります。ほとんどの場合、化学薬品を注いだボトルのラベルまたは問題から初期濃度を知っています。
この数値に100を掛けます。これは、イオン化の程度を表すパーセンテージです。
ヒント
